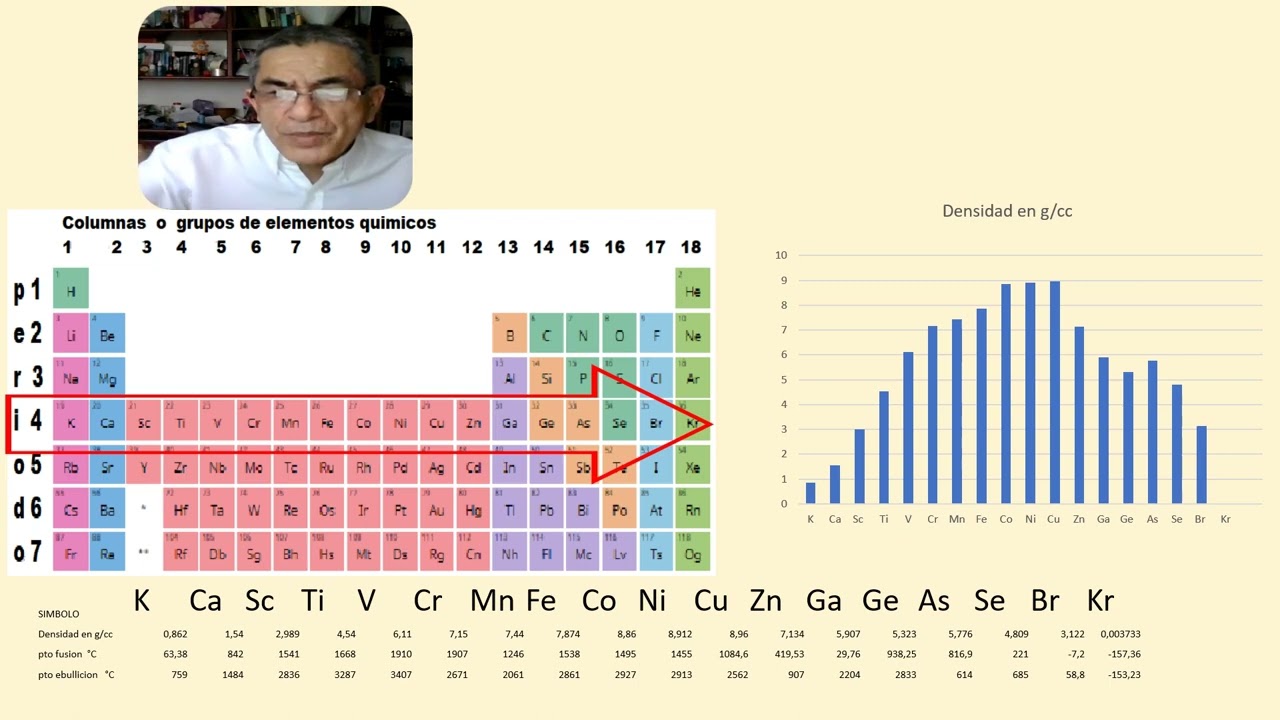
| Tabla Periódica Completa: Puntos de Fusión y Ebullición de Elementos Químicos |
Introducción a los Puntos de Fusión y Ebullición
¿Alguna vez te has preguntado por qué el agua hierve a 100 grados Celsius mientras que el hierro se funde a más de 1500 grados? La tabla periódica no solo es un mapa fascinante de los elementos químicos, sino que también nos ofrece una gran cantidad de información sobre las propiedades físicas de estos elementos, incluyendo sus puntos de fusión y ebullición. Estos dos conceptos son fundamentales en la química y en nuestra vida diaria, ya que nos ayudan a entender cómo se comportan los materiales en diferentes condiciones. Así que, ¡abrocha tu cinturón y acompáñame en este recorrido por el mundo de los elementos químicos y sus propiedades térmicas!
¿Qué Son el Punto de Fusión y el Punto de Ebullición?
Empecemos por aclarar qué significan estos términos. El punto de fusión es la temperatura a la que un sólido se convierte en líquido. Imagina que tienes un delicioso chocolate en una barra: a medida que lo calientas, eventualmente se derrite y se convierte en un líquido viscoso. Esa temperatura en la que el chocolate pasa de sólido a líquido es su punto de fusión. Por otro lado, el punto de ebullición es la temperatura a la que un líquido se transforma en vapor. Siguiendo con el ejemplo del agua, cuando la calientas en una olla, eventualmente comienza a burbujear y se convierte en vapor; esa es su temperatura de ebullición.
¿Por Qué Son Importantes Estas Propiedades?
Las propiedades de fusión y ebullición son cruciales no solo en la química, sino también en la ingeniería, la cocina y muchas otras áreas. Por ejemplo, al diseñar un motor, los ingenieros deben considerar los puntos de ebullición de los líquidos de refrigeración para asegurarse de que no se evaporen durante el funcionamiento. En la cocina, entender cómo y cuándo un ingrediente cambia de estado puede marcar la diferencia entre un plato delicioso y uno arruinado. Entonces, sí, estos conceptos son más relevantes de lo que podrías pensar.
¿Cómo Se Determinan Estos Puntos?
Los puntos de fusión y ebullición no son solo números aleatorios que se encuentran en un libro de texto. Se determinan a través de experimentos meticulosos. Por lo general, se utilizan calorímetros para medir la temperatura exacta en la que un material cambia de estado. ¿Sabías que algunos elementos tienen puntos de fusión y ebullición extremadamente altos? Por ejemplo, el tungsteno tiene un punto de fusión de aproximadamente 3422 grados Celsius, lo que lo convierte en uno de los metales más resistentes al calor.
Factores que Afectan los Puntos de Fusión y Ebullición
Varios factores pueden influir en estas temperaturas. Uno de los más importantes es la presión. En un entorno de alta presión, los líquidos pueden hervir a temperaturas más altas. Por eso, en las montañas, donde la presión atmosférica es más baja, el agua hierve a temperaturas más bajas que a nivel del mar. También la estructura molecular de una sustancia juega un papel crucial. Los enlaces químicos más fuertes entre las moléculas generalmente resultan en puntos de fusión y ebullición más altos. ¡Es como si las moléculas estuvieran sosteniendo una fiesta y las más fuertes se negaran a dejar entrar a los débiles!
Ejemplos de Elementos y Sus Propiedades
Ahora que hemos establecido las bases, hablemos de algunos elementos específicos y sus puntos de fusión y ebullición. Vamos a explorar algunos metales, no metales y gases.
Metales
1. Hierro (Fe): Este metal tan común tiene un punto de fusión de 1538 °C y un punto de ebullición de 2862 °C. Por eso, se utiliza en la construcción de estructuras sólidas.
2. Oro (Au): El oro, conocido por su belleza y valor, se funde a 1064 °C y hierve a 2856 °C. Su alta resistencia a la corrosión lo convierte en un material ideal para joyería.
No Metales
1. Carbono (C): En su forma de grafito, el carbono tiene un punto de fusión de 3652 °C, pero no tiene un punto de ebullición definido, ya que se sublima a temperaturas más altas.
2. Azufre (S): Este elemento tiene un punto de fusión de 115 °C y un punto de ebullición de 445 °C. El azufre es conocido por su característico olor a huevos podridos.
Gases
1. Oxígeno (O2): Este gas vital tiene un punto de fusión de -218.8 °C y un punto de ebullición de -182.9 °C. Por eso, en condiciones normales, lo encontramos en estado gaseoso.
2. Nitrógeno (N2): Al igual que el oxígeno, el nitrógeno también es un gas a temperatura ambiente, con un punto de fusión de -210 °C y un punto de ebullición de -195.8 °C.
Tabla Resumen de Puntos de Fusión y Ebullición
Para que tengas una referencia rápida, aquí tienes una pequeña tabla con algunos elementos y sus respectivos puntos de fusión y ebullición:
| Elemento | Punto de Fusión (°C) | Punto de Ebullición (°C) |
|---|---|---|
| Hierro (Fe) | 1538 | 2862 |
| Oro (Au) | 1064 | 2856 |
| Carbono (C) | 3652 | No definido |
| Azufre (S) | 115 | 445 |
| Oxígeno (O2) | -218.8 | -182.9 |
| Nitrógeno (N2) | -210 | -195.8 |
Aplicaciones Prácticas de Conocer Estos Puntos
Ahora que hemos cubierto la teoría, hablemos de cómo este conocimiento se aplica en el mundo real. Desde la industria hasta la cocina, los puntos de fusión y ebullición son esenciales. Por ejemplo, en la industria de alimentos, la temperatura a la que se cocina un alimento puede cambiar su textura y sabor. Si un chef sabe el punto de fusión de la mantequilla, puede utilizarla para obtener la consistencia perfecta en una salsa.
Además, en la industria química, se utilizan estas propiedades para separar compuestos. En un proceso llamado destilación, se calienta una mezcla hasta que uno de los componentes alcanza su punto de ebullición, se convierte en vapor y luego se enfría para volver a convertirlo en líquido, separándolo de los otros componentes. ¡Es como magia científica!
Conclusiones
En resumen, los puntos de fusión y ebullición son más que simples números en una tabla; son conceptos que influyen en nuestra vida diaria de maneras que a menudo no consideramos. Desde la construcción de edificios hasta la preparación de nuestras comidas favoritas, entender estas propiedades nos permite tomar decisiones más informadas. Así que la próxima vez que veas un elemento en la tabla periódica, recuerda que hay mucho más detrás de esos números. ¡Espero que hayas disfrutado de este viaje a través del mundo de los elementos químicos!
Preguntas Frecuentes
1. ¿Por qué el agua hierve a diferentes temperaturas en distintas altitudes?
La temperatura de ebullición del agua disminuye a medida que la presión atmosférica disminuye. Por eso, en lugares altos, como las montañas, el agua hierve a temperaturas más bajas.
2. ¿Todos los elementos tienen un punto de fusión y un punto de ebullición?
Sí, todos los elementos tienen estas propiedades, pero algunos pueden no tener un punto de ebullición definido, como el carbono en forma de grafito, que sublima en lugar de hervir.
3. ¿Cómo afecta la presión a los puntos de fusión y ebullición?
La presión puede aumentar o disminuir los puntos de fusión y ebullición. A mayor presión, los líquidos tienden a hervir a temperaturas más altas, mientras que a menor presión, hierven a temperaturas más bajas.
4. ¿Por qué algunos metales tienen puntos de fusión tan altos?
Los metales con puntos de fusión altos, como el tungsteno, tienen enlaces metálicos muy fuertes entre sus átomos, lo que requiere más energía (calor) para romper esos enlaces y cambiar de estado.
5. ¿Cómo se utilizan los puntos de fusión y ebullición en la industria?
Estos puntos son cruciales para procesos industriales como la destilación, la separación de compuestos químicos y en la fabricación de materiales que deben resistir altas temperaturas.