Cómo se Forma un Enlace Metálico: Proceso y Características Clave
Introducción al Enlace Metálico
¿Alguna vez te has preguntado por qué los metales tienen propiedades tan singulares? Desde su brillo hasta su maleabilidad, todo se debe a un fenómeno fascinante: el enlace metálico. Este tipo de enlace es un pilar fundamental en la química de los metales y es responsable de muchas de sus características únicas. Pero, ¿qué es exactamente un enlace metálico? En este artículo, te llevaré a través del proceso de formación de un enlace metálico y exploraremos sus características clave. Así que, siéntate, relájate y acompáñame en este viaje por el mundo de la química metálica.
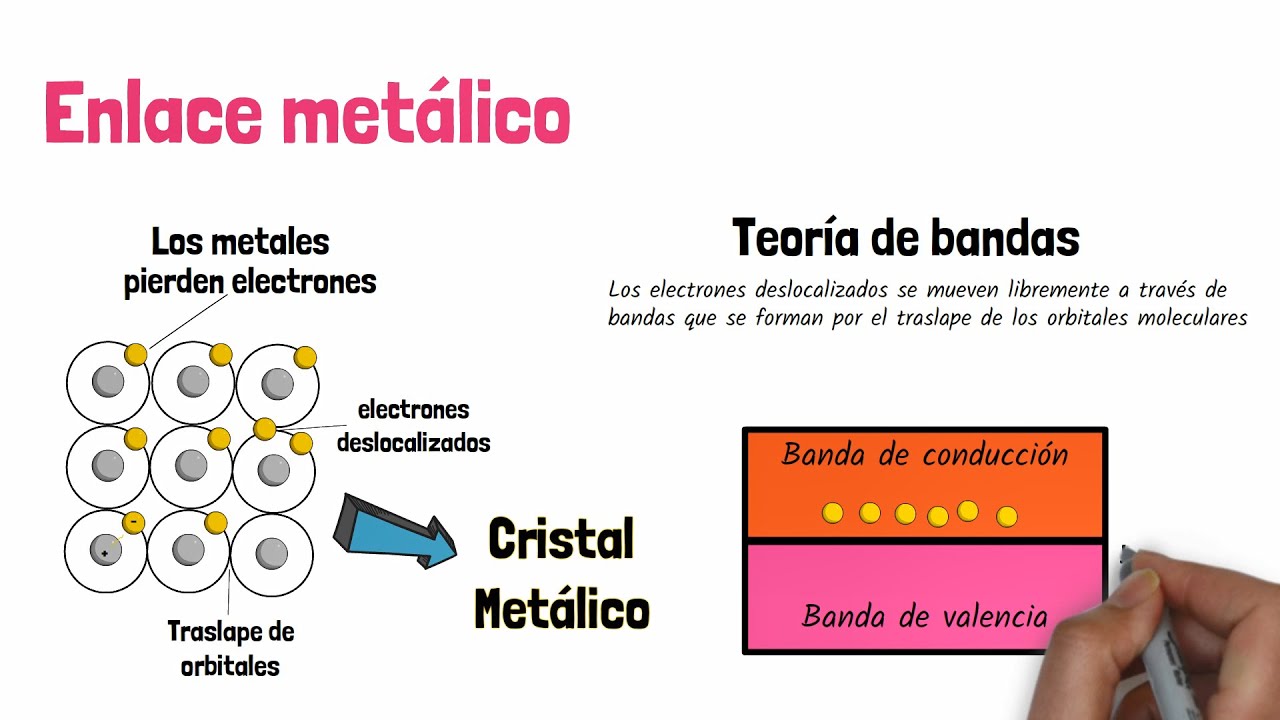
Los enlaces metálicos se forman cuando los átomos de un metal se agrupan y comparten sus electrones de una manera muy especial. Imagina una gran fiesta donde todos los asistentes, en este caso los electrones, están bailando libremente. A diferencia de los enlaces covalentes, donde los electrones son compartidos de manera más estricta entre dos átomos, en un enlace metálico los electrones se mueven libremente entre un grupo de átomos, creando lo que se conoce como un «mar de electrones». Este concepto es fundamental para entender cómo los metales pueden conducir electricidad y calor, además de ser maleables y dúctiles.
La Estructura de los Metales
Para entender mejor cómo se forma un enlace metálico, primero debemos echar un vistazo a la estructura de los metales. Los átomos metálicos se organizan en un patrón regular y repetitivo, formando lo que se conoce como una red cristalina. Esta red es como un rompecabezas tridimensional donde cada pieza es un átomo de metal. En el centro de cada átomo, encontramos protones y neutrones, pero lo que realmente nos interesa son los electrones que orbitan alrededor del núcleo.
Los Electrones de Valencia
Los electrones de valencia son aquellos que se encuentran en la capa más externa de un átomo y son los responsables de las interacciones químicas. En el caso de los metales, estos electrones son relativamente pocos y se encuentran débilmente unidos al núcleo. Esto significa que pueden ser fácilmente liberados y compartidos con otros átomos metálicos. Cuando los átomos se agrupan, estos electrones de valencia se desprenden y se convierten en un «mar de electrones» que fluye entre los núcleos positivos de los átomos metálicos.
El Proceso de Formación del Enlace Metálico
Ahora que tenemos una idea básica de la estructura de los metales, es hora de adentrarnos en el proceso de formación del enlace metálico. Este proceso se puede dividir en varias etapas.
1. Desprendimiento de Electrones
El primer paso en la formación de un enlace metálico es el desprendimiento de los electrones de valencia. Cuando los átomos metálicos se acercan, los electrones de valencia de cada átomo comienzan a liberarse. Este desprendimiento es crucial, ya que permite que los electrones se muevan libremente en el espacio entre los núcleos atómicos.
2. Creación del Mar de Electrones
Una vez que los electrones de valencia se han desprendido, forman un «mar de electrones». Este mar no es solo una metáfora; realmente se comporta como un fluido que rodea a los núcleos positivos de los átomos metálicos. Esta nube de electrones permite que los núcleos se mantengan unidos, a pesar de que están repeliéndose entre sí debido a sus cargas positivas. Es como un grupo de amigos que, aunque pueden tener diferencias, se mantienen unidos por la conexión que comparten.
3. Atracción entre Núcleos y Electrones
El siguiente paso en la formación del enlace metálico es la atracción entre los núcleos positivos de los átomos metálicos y el mar de electrones que los rodea. Esta atracción es lo que da estabilidad a la estructura metálica. Aunque los núcleos se repelen entre sí, la fuerza de atracción entre los electrones y los núcleos es lo suficientemente fuerte como para mantener la estructura unida. Aquí es donde entra en juego la magia del enlace metálico.
Características Clave del Enlace Metálico
Ahora que hemos explorado el proceso de formación del enlace metálico, es importante discutir algunas de sus características clave que hacen que los metales sean tan únicos.
Conducción de Electricidad y Calor
Una de las propiedades más notables de los metales es su capacidad para conducir electricidad y calor. Esto se debe a la presencia del mar de electrones. Cuando se aplica un voltaje, los electrones libres pueden moverse rápidamente a través del metal, permitiendo que la electricidad fluya. De manera similar, cuando se calienta un metal, los electrones pueden transferir energía térmica a través del material, lo que lo convierte en un excelente conductor de calor.
Maleabilidad y Ductilidad
Otra característica fascinante de los metales es su maleabilidad y ductilidad. La maleabilidad se refiere a la capacidad de un metal para ser moldeado en formas delgadas y planas, mientras que la ductilidad se refiere a la capacidad de ser estirado en hilos. Estas propiedades se deben a la naturaleza del enlace metálico. Cuando se aplica una fuerza a un metal, los átomos pueden deslizarse unos sobre otros sin romper el enlace, gracias a la flexibilidad del mar de electrones.
Brillo Metálico
Si alguna vez has admirado el brillo de un metal pulido, has sido testigo de otra propiedad del enlace metálico. Este brillo se debe a la capacidad de los electrones libres de reflejar la luz. Cuando la luz incide sobre la superficie de un metal, los electrones en el mar responden a la luz y la reflejan, creando ese resplandor característico que asociamos con los metales.
Ejemplos de Enlaces Metálicos en la Naturaleza
Es interesante notar que los enlaces metálicos no son solo una curiosidad científica; están presentes en muchos materiales que usamos en nuestra vida diaria. Algunos ejemplos incluyen:
El Hierro
El hierro es un metal que se utiliza en la construcción y en la fabricación de herramientas. Su estructura de enlace metálico le proporciona la resistencia necesaria para soportar cargas pesadas, lo que lo convierte en un material esencial en la industria de la construcción.
El Cobre
El cobre es conocido por su excelente conductividad eléctrica, lo que lo convierte en un material ideal para cables eléctricos. Su capacidad para formar enlaces metálicos le permite conducir la electricidad de manera eficiente, lo que es crucial en el mundo moderno.
El Aluminio
El aluminio es otro ejemplo de un metal con enlaces metálicos. Su ligereza y resistencia lo hacen popular en la fabricación de aviones y automóviles. Además, su maleabilidad permite que se pueda moldear en diversas formas sin romperse.
Preguntas Frecuentes
¿Por qué los metales son buenos conductores de electricidad?
Los metales son buenos conductores de electricidad debido a la presencia de electrones libres en su estructura. Estos electrones pueden moverse fácilmente, permitiendo que la corriente eléctrica fluya a través del material.
¿Qué diferencia hay entre un enlace metálico y un enlace covalente?
La principal diferencia radica en cómo se comparten los electrones. En un enlace covalente, los electrones son compartidos entre dos átomos específicos, mientras que en un enlace metálico, los electrones se mueven libremente entre muchos átomos, formando un mar de electrones.
¿Por qué los metales son maleables y dúctiles?
Los metales son maleables y dúctiles debido a la flexibilidad del enlace metálico. Cuando se aplica presión, los átomos pueden deslizarse unos sobre otros sin romper el enlace, lo que permite que el metal se moldee sin fracturarse.
¿Cómo se relaciona la estructura cristalina con las propiedades metálicas?
La estructura cristalina de los metales permite que los átomos se alineen de manera ordenada, lo que contribuye a la fuerza y estabilidad del enlace metálico. Esta organización facilita la movilidad de los electrones, mejorando las propiedades de conducción y maleabilidad.
¿Los enlaces metálicos son permanentes?
Sí, los enlaces metálicos son generalmente fuertes y permanentes, lo que permite que los metales mantengan su forma y propiedades bajo condiciones normales. Sin embargo, pueden romperse si se aplican fuerzas extremas o altas temperaturas.
En resumen, los enlaces metálicos son un fenómeno fascinante que explica muchas de las propiedades de los metales. Desde su capacidad para conducir electricidad hasta su maleabilidad y brillo, estos enlaces son fundamentales para entender cómo interactúan los átomos metálicos entre sí. Espero que este artículo te haya ayudado a comprender mejor este tema tan interesante. ¿Tienes alguna otra pregunta sobre enlaces metálicos? ¡Déjamelo saber!